1. ¿Qué son los probióticos? Una definición científica a nivel de cepa
Aunque el término "probióticos" se ha popularizado en productos de consumo, su definición científica es mucho más específica y restrictiva de lo que la mayoría cree. Según la FAO/OMS, los probióticos son microorganismos vivos que, administrados en cantidades adecuadas, aportan un beneficio para la salud . Cada parte de esta definición tiene un peso científico real.
Los probióticos deben estar vivos al consumirse . Esto parece obvio, pero muchos productos comerciales no garantizan su supervivencia durante la fabricación, el transporte y el almacenamiento. La actividad biológica de un probiótico depende de su capacidad para soportar condiciones gástricas adversas (como el ácido estomacal, las sales biliares y las enzimas digestivas) antes de llegar vivos a los intestinos. Las bacterias muertas o los fragmentos posbióticos aún pueden tener algunos efectos fisiológicos, pero no pueden clasificarse como probióticos según la definición estricta.
Los probióticos deben tomarse en dosis adecuadas , comúnmente medidas en UFC (unidades formadoras de colonias). Distintas cepas requieren diferentes umbrales mínimos para producir efectos mensurables. Un producto que presume de contener "millones de bacterias vivas" es prácticamente inútil; los efectos clínicos significativos suelen observarse en miles de millones .
Y lo más importante: los probióticos deben definirse a nivel de cepa . Esto significa que el nombre científico completo debe incluir género, especie y un código alfanumérico de cepa. Por ejemplo:
Lactobacillus rhamnosus = especie
Lactobacillus rhamnosus GG (ATCC 53103) = cepa específica con beneficios comprobados
Dos organismos pueden compartir el mismo género y especie, pero comportarse como entidades biológicas completamente distintas si tienen identificadores de cepa distintos. Por eso, afirmaciones como «El Lactobacillus mejora la digestión» carecen de validez científica. Solo la evidencia específica de cada cepa puede establecer un beneficio real para la salud.
En pocas palabras: el número de cepa es la diferencia entre un probiótico validado científicamente y cualquier otra bacteria cualquiera.
Este nivel de precisión es lo que separa a los suplementos probióticos de alta calidad de los vagos productos de “cultivo vivo” o alimentos fermentados que no se someten a pruebas clínicas controladas.
2. El microbioma humano: el ecosistema que apoyan los probióticos
Para comprender la función de los probióticos, primero debemos comprender el sistema con el que interactúan: el microbioma humano . Tan solo el intestino humano contiene billones de microorganismos (bacterias, hongos, virus y arqueas) que forman una compleja comunidad ecológica mucho mayor que la cantidad de células humanas en todo el cuerpo. Este ecosistema es dinámico, diverso y está profundamente integrado en la fisiología humana.
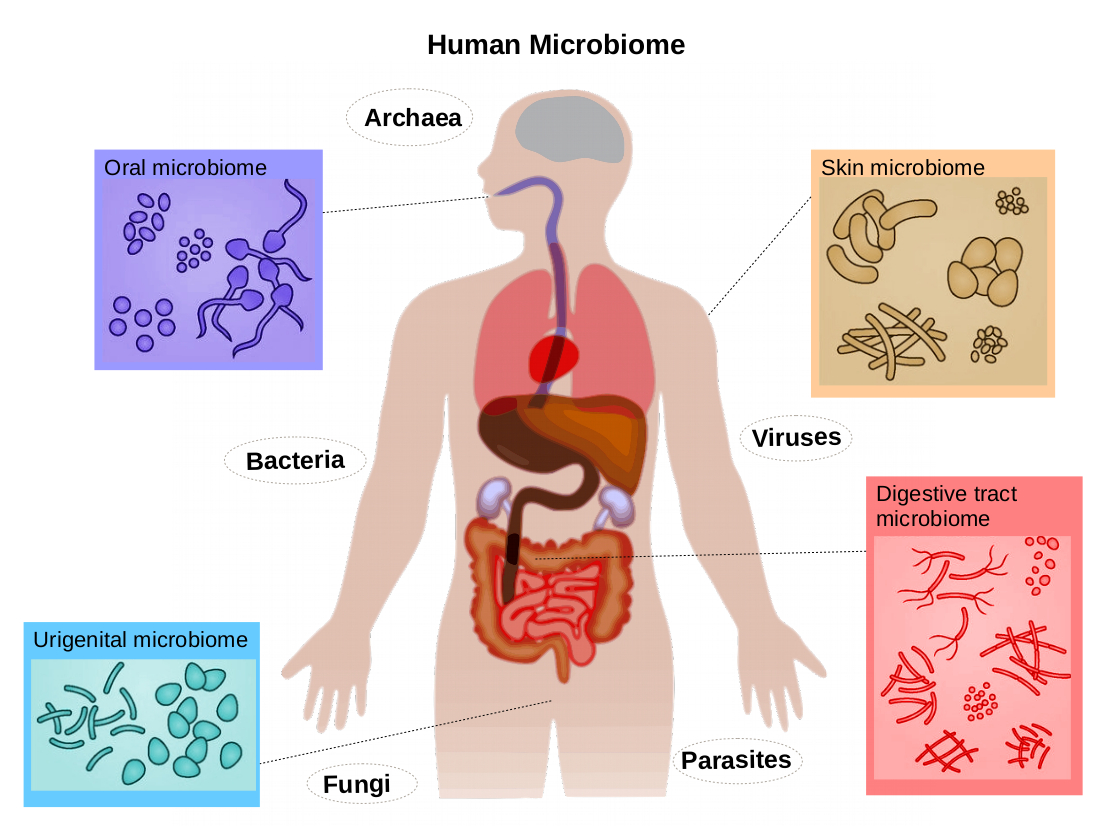
El microbioma intestinal participa en cientos de funciones críticas:
Digerir las fibras dietéticas que las enzimas humanas no pueden descomponer.
Producción de ácidos grasos de cadena corta (AGCC) que alimentan las células del colon
Sintetizar vitaminas como la vitamina K y algunas vitaminas del complejo B.
Entrenar al sistema inmunológico para distinguir amenazas de estímulos inofensivos
Regulación de la inflamación en todo el cuerpo.
Comunicarse con el cerebro a través de señales neuronales, hormonales y bioquímicas.
Influye en el metabolismo , el azúcar en sangre, los niveles de lípidos y el almacenamiento de grasa.
Un ecosistema intestinal sano es como un bosque próspero: altamente diverso, equilibrado y resiliente. Sin embargo, los estilos de vida modernos pueden alterar fácilmente este equilibrio. Una dieta rica en alimentos ultraprocesados, el estrés crónico, la falta de sueño, el uso de antibióticos, el consumo de alcohol o las infecciones gastrointestinales pueden causar disbiosis , es decir, un desequilibrio en la composición microbiana.
La disbiosis no es un problema menor; ahora está relacionada con:
Síndrome del intestino irritable (SII)
Enfermedades inflamatorias del intestino
Obesidad y síndrome metabólico
Ansiedad, depresión y cambios cognitivos
Problemas de la piel como eczema, acné y rosácea.
Alergias y reacciones autoinmunes
En este contexto, los probióticos no funcionan como remedios milagrosos, sino como herramientas biológicas diseñadas para ayudar a restablecer el equilibrio ecológico . No pueden solucionarlo todo por sí solos, pero, si se seleccionan correctamente, influyen en este complejo entorno de maneras que contribuyen significativamente a la salud humana.
3. Cómo funcionan los probióticos: mecanismos detallados
La mayoría de los artículos básicos resumen los mecanismos probióticos en una sola frase: “Los probióticos ayudan a restablecer el equilibrio intestinal y refuerzan la inmunidad”.
Esto es una simplificación excesiva que resulta engañosa. A continuación, se presenta un análisis completo, mecanismo por mecanismo , escrito desde la perspectiva de alguien que diseña fórmulas, no de alguien que navega por el supermercado.
Exclusión competitiva: los probióticos ocupan un lugar destacado antes que los patógenos
En el intestino, los microbios compiten por espacio físico en la mucosa intestinal. Esta superficie es limitada, lo que significa que los organismos que se adhieren primero obtienen la ventaja. Ciertas cepas probióticas poseen proteínas de adhesión especializadas que les permiten anclarse con mayor eficacia que las bacterias dañinas.
Al ocupar estos sitios de unión, los probióticos impiden que las especies patógenas establezcan colonias, un fenómeno conocido como exclusión competitiva .
Por qué esto es importante:
Reduce el crecimiento excesivo de patógenos
Protege contra alteraciones post-antibióticos
Minimiza los episodios de diarrea o problemas digestivos del viajero.
Este mecanismo es especialmente importante inmediatamente después del tratamiento con antibióticos, cuando el espacio microbiano está plenamente abierto a la recolonización.
Producción de ácidos orgánicos: creación de un entorno perjudicial para las bacterias dañinas
Muchas cepas de Lactobacillus y Bifidobacterium fermentan carbohidratos para producir ácido láctico , ácido acético y otros metabolitos que reducen el pH del entorno intestinal.
Las bacterias patógenas, como E. coli , Clostridium y Salmonella , prefieren un entorno más alcalino, por lo que un intestino ligeramente ácido restringe su proliferación.
Esta acidificación:
Mejora la absorción de nutrientes.
Mejora la solubilidad de los minerales.
Limita el crecimiento de microbios dañinos.
Favorece una sucesión microbiana más saludable
En la práctica, esto significa que los probióticos no “matan” las bacterias dañinas como lo hacen los antibióticos, sino que las superan y las matan de hambre alterando el medio ambiente.
Modulación inmunitaria: los probióticos no refuerzan la inmunidad, la equilibran
El intestino es el órgano inmunitario más grande del cuerpo humano. Alrededor del 70 % de las células inmunitarias residen en el tracto gastrointestinal. Los probióticos interactúan con las células inmunitarias a través de receptores de reconocimiento de patrones, señalización de citocinas y subproductos moleculares.
Pero los probióticos no simplemente “refuerzan la inmunidad”.
Actúan como moduladores inmunes , lo que significa:
Mejorar la inmunidad hipoactiva
Calmar las respuestas inflamatorias hiperactivas
Mejora de la secreción de IgA en la superficie de la mucosa
Ajuste de las respuestas de las células T para reducir la hipersensibilidad
Este doble efecto explica por qué los probióticos son útiles en condiciones que parecen contradictorias:
Apoyando la resistencia a las infecciones
Alivio de los síntomas del eczema y la alergia
Mantener el equilibrio inmunológico durante el estrés
Todo es parte del mismo mecanismo regulador, no un efecto contradictorio.
Fortalecimiento de la barrera intestinal: protección contra el síndrome del intestino permeable
La barrera intestinal se mantiene unida por proteínas llamadas uniones estrechas , que regulan lo que entra al torrente sanguíneo. Cuando esta barrera se debilita (debido al estrés, toxinas, inflamación, mala alimentación o alcohol), las partículas que deberían permanecer dentro del intestino se filtran a la circulación sistémica. Esto desencadena una inflamación crónica leve, a menudo llamada endotoxemia metabólica .
Se ha demostrado que ciertas cepas probióticas:
Aumentar la expresión de proteínas de unión estrecha
Estimular la producción de mucina
Apoyar la regeneración epitelial
Reducir la permeabilidad (“intestino permeable”)
Una barrera intestinal más saludable no solo mejora la digestión sino que también reduce la inflamación sistémica, lo que impacta la salud de la piel, la estabilidad metabólica e incluso el estado de ánimo.
Mejora de la producción de SCFA: combustible para las células del colon y la salud a largo plazo
Los ácidos grasos de cadena corta (AGCC), especialmente el butirato , se producen cuando las bacterias intestinales fermentan fibras y prebióticos. Butirato:
Es la principal fuente de energía para las células del colon.
Reduce la inflamación
Mejora la función metabólica
Apoya la sensibilidad a la insulina
Afecta la síntesis de neurotransmisores
Ayuda a regular el apetito y la saciedad.
Los probióticos a menudo funcionan en conjunto con la fibra dietética:
Ayudan a fermentar las fibras con mayor eficiencia, aumentando la producción de AGCC. Esta es una de las razones por las que los simbióticos (probióticos + prebióticos) suelen ser más eficaces que los probióticos solos.
Eje intestino-cerebro: cómo influyen los microbios en el estado de ánimo, el estrés y el sueño
El intestino produce aproximadamente el 90% de la serotonina del cuerpo , y los metabolitos microbianos influyen en las vías de los neurotransmisores, el nervio vago y los canales inflamatorios, tres de los impulsores más importantes de la salud mental y emocional.
Se ha demostrado que ciertas cepas (por ejemplo, Lactobacillus helveticus R0052 y Bifidobacterium longum R0175):
Reducir el cortisol
Mejorar la resiliencia al estrés
Apoya la calidad del sueño
Influir en el procesamiento emocional
Esta área de investigación se conoce como psicobiótica , uno de los campos de más rápido desarrollo en la ciencia del microbioma.
Regulación metabólica: el vínculo microbiano con el peso y el azúcar en sangre
Los probióticos influyen en el metabolismo indirectamente a través de:
Reducción de la permeabilidad intestinal → menos inflamación
Hormonas moduladoras como el GLP-1
Afecta la eficiencia de absorción de grasas
Regulación del metabolismo de los ácidos biliares
Influencia en la relación Firmicutes/Bacteroidetes
Los probióticos por sí solos no provocan una pérdida de peso espectacular, pero contribuyen a un entorno metabólico que favorece:
Mejor control de la glucosa
Inflamación reducida
Acumulación de grasa visceral inferior
Beneficios clínicos de los probióticos
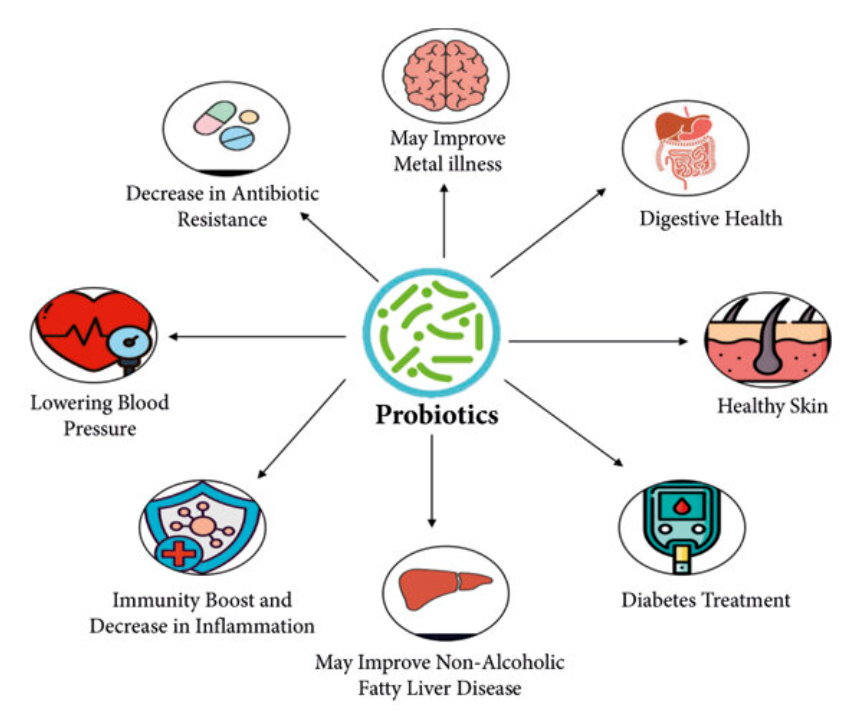
Los probióticos influyen en la salud humana en un amplio espectro de sistemas fisiológicos. Sus efectos son muy específicos de cada cepa , lo que significa que cada una presenta mecanismos, evidencia clínica y valor terapéutico diferentes. A continuación, se presenta un desglose completo, categoría por categoría, de los beneficios de los probióticos, redactado con detalles de calidad médica y relevancia práctica tanto para las marcas de suplementos como para los consumidores.
1. Salud digestiva: el beneficio más establecido y ampliamente estudiado
La salud digestiva sigue siendo la aplicación más validada científicamente de los probióticos, ya que la microbiota intestinal influye directamente en la motilidad, la absorción de nutrientes, la actividad inmunitaria y la integridad de la mucosa. La disbiosis —a menudo causada por antibióticos, estrés, mala alimentación, infecciones o inflamación crónica— puede manifestarse como estreñimiento, diarrea, distensión abdominal, dolor abdominal o deposiciones irregulares.
Los probióticos promueven la estabilidad digestiva a través de varios mecanismos: regulando la motilidad, desplazando los microbios productores de gases, fortaleciendo las barreras mucosas, reduciendo la inflamación y restaurando la diversidad microbiana.
1.1 Síndrome del intestino irritable (SII)
El síndrome del intestino irritable afecta a millones de personas en todo el mundo e implica una interacción compleja de hipersensibilidad visceral, activación inmunitaria, disbiosis y estrés.
Múltiples ECA demuestran que cepas específicas pueden mejorar los síntomas del SII al:
reducir el dolor abdominal
mejorar la regularidad intestinal
Disminuir la hinchazón
modulación de biomarcadores inflamatorios
Las cepas altamente estudiadas incluyen:
Lactobacillus plantarum 299v: mejora el dolor abdominal y la tolerancia a los gases.
Bifidobacterium infantis 35624: reduce la hinchazón, el dolor y la irregularidad intestinal.
Saccharomyces boulardii CNCM I-745: reduce los síntomas del síndrome del intestino irritable con predominio de diarrea.
Estas cepas actúan a través de la actividad antiinflamatoria, la mejora de los SCFA y la modulación inmunitaria del huésped.
1.2 Estreñimiento (Estreñimiento funcional y tránsito lento)
El estreñimiento frecuentemente surge de una producción inadecuada de SCFA, motilidad deteriorada o diversidad microbiana reducida.
Los probióticos pueden estimular el peristaltismo produciendo metabolitos que interactúan con el sistema nervioso entérico.
Cepas con fuerte evidencia:
Bifidobacterium lactis BB-12: aumenta la frecuencia de las deposiciones y mejora su forma.
Lactobacillus casei Shirota: mejora la motilidad y reduce el tiempo de tránsito intestinal.
Lactobacillus rhamnosus GG: útil tanto para adultos como para niños
Los probióticos a menudo funcionan sinérgicamente con los prebióticos (FOS, inulina) para mejorar los hábitos intestinales.
1.3 Diarrea, incluida la diarrea asociada a antibióticos (DAA)
Uno de los usos clínicos más probados de los probióticos es la prevención de la DAA, en la que los antibióticos alteran la flora intestinal normal y permiten que proliferen patógenos oportunistas.
Las cepas más estudiadas incluyen:
Saccharomyces boulardii CNCM I-745: el estándar de oro para la prevención de la DAA
Lactobacillus rhamnosus GG: reduce la incidencia y la duración
Cepa de Bifidobacterium breve Yakult: estabiliza el equilibrio microbiano durante la terapia con antibióticos
Estas cepas exhiben actividades de inhibición de patógenos, normalización de la señalización inmune y neutralización de toxinas.
1.4 Hinchazón, gases y dispepsia
La producción de gases y la distensión abdominal a menudo son resultado de desequilibrios de la fermentación o cambios transitorios en la microbiota.
Cepas útiles:
Lactobacillus plantarum 299v
Bifidobacterium longum NCC3001 – reduce la hipersensibilidad visceral
Lactobacillus acidophilus NCFM
Estas cepas mejoran la tolerancia a los gases, reducen el estrés de la fermentación y mejoran la resiliencia de la mucosa.
2. Apoyo inmunitario: Equilibrar, no “reforzar” la inmunidad
El sistema inmunitario y la microbiota intestinal mantienen una comunicación constante. Los probióticos influyen en la inmunidad modulando las vías inflamatorias, mejorando la defensa de los anticuerpos de la mucosa y estabilizando la señalización inmunitaria intestinal. En lugar de fortalecer la inmunidad indiscriminadamente, los probióticos optimizan la respuesta inmunitaria , reduciendo la inflamación excesiva y mejorando la resistencia a los patógenos.
Los principales beneficios inmunológicos incluyen:
Reducción de la frecuencia y gravedad de los resfriados comunes
Mejora la secreción de IgA en la mucosa
Menos inflamación en el tracto gastrointestinal
Recuperación más rápida de las infecciones
Respuesta mejorada a las vacunas en ciertas poblaciones
Cepas con evidencia:
Lactobacillus paracasei CASEI 431: mejora la respuesta inmunitaria a las vacunas
Bifidobacterium animalis BB-12: mejora la inmunidad de las mucosas
Lactobacillus rhamnosus GG: reduce las infecciones respiratorias en niños
Lactobacillus casei Shirota: modula la actividad de las células NK
Estas cepas no estimulan agresivamente el sistema inmunológico, sino que lo guían hacia el equilibrio, reduciendo la sobreactivación innecesaria y mejorando al mismo tiempo la defensa de primera línea.
3. Salud femenina: microbioma vaginal y apoyo del tracto urinario
El microbioma vaginal femenino está dominado por especies de Lactobacillus, que mantienen un ambiente ácido (pH óptimo ≈ 4,5) mediante la producción de ácido láctico. El estrés, los cambios hormonales, los antibióticos y la actividad sexual pueden alterar este ecosistema, aumentando el riesgo de vaginosis bacteriana, infecciones por hongos y molestias urinarias.
Los probióticos favorecen la salud de la mujer al:
Restaurando el predominio de Lactobacillus
Reducir el pH vaginal
Producción de peróxido de hidrógeno para inhibir patógenos.
Fortalecimiento de las barreras mucosas
Reducción de la recurrencia de la vaginosis bacteriana (VB)
Cepas clínicamente significativas:
Lactobacillus crispatus CTV-05: el estándar de oro para la restauración del microbioma vaginal
Lactobacillus rhamnosus GR-1 + Lactobacillus reuteri RC-14: par sinérgico ampliamente validado en estudios
Lactobacillus jensenii : favorece la integridad de la mucosa.
Estas cepas pueden tomarse por vía oral o administrarse por vía intravaginal dependiendo del contexto clínico.
4. Salud de la piel: el eje intestino-piel
La piel y el intestino comparten fuertes conexiones inmunológicas y metabólicas. La disbiosis puede aumentar la inflamación sistémica, debilitar la barrera epitelial y promover afecciones como el acné, el eccema y el enrojecimiento.
Los probióticos pueden beneficiar la piel al:
Reducción de las citocinas inflamatorias
Apoyando la integridad de la barrera intestinal
Modulación de la producción de sebo
Equilibrio de los metabolitos microbianos asociados con los brotes de la piel
Mejorar la retención de humedad de la piel.
Cepas implicadas en beneficios para la piel:
Lactobacillus rhamnosus GG: reduce el riesgo de eczema en bebés y niños
Bifidobacterium longum : disminuye la sensibilidad y la inflamación.
Lactobacillus paracasei ST11: ayuda a la barrera cutánea y a la hidratación.
Si bien los probióticos no son una panacea, favorecen el equilibrio interno que se refleja externamente en la salud de la piel.
5. El eje intestino-cerebro: probióticos para el estado de ánimo, el estrés y la función cognitiva
Una de las áreas más apasionantes y de más rápida evolución de la investigación sobre probióticos es el eje microbiota-intestino-cerebro , una red de comunicación que involucra el nervio vago, los neurotransmisores, la señalización inmune y los metabolitos microbianos.
Actualmente se reconoce que la disbiosis es un factor que contribuye a:
Ansiedad
Sensibilidad al estrés
Mal sueño
Niebla cognitiva
Síntomas depresivos leves
Las cepas psicobióticas con evidencia incluyen:
Lactobacillus helveticus R0052 + Bifidobacterium longum R0175: reducen el cortisol y mejoran la respuesta al estrés.
Bifidobacterium longum NCC3001: mejora el procesamiento emocional
Lactobacillus plantarum PS128: evidencia emergente de la regulación del estado de ánimo
Estas cepas influyen en las vías de la serotonina, la señalización de GABA, la inflamación y el nervio vago.
6. Probióticos para la salud metabólica y el control del peso
Aunque los probióticos no son medicamentos para bajar de peso, influyen en la regulación metabólica a través de varias vías:
Reducir la permeabilidad intestinal (reducir la inflamación sistémica)
Modulación del GLP-1 y las hormonas del apetito
Afecta el metabolismo de los triglicéridos
Influir en el almacenamiento de grasa y el gasto energético
Apoyando un mejor control del azúcar en sangre
Cepas destacadas:
Lactobacillus gasseri SBT2055 – asociado con la reducción de la grasa visceral
Bifidobacterium breve B-3: vinculada a una mejor composición corporal
Cepas de Lactobacillus plantarum : favorecen el equilibrio metabólico
Estos efectos son modestos pero significativos cuando se combinan con intervenciones en la dieta y el estilo de vida.
7. Probióticos en las diferentes etapas de la vida: bebés, adultos y personas mayores
Bebés
Los primeros 1000 días de vida son fundamentales para la formación del microbioma.
Los probióticos pueden ayudar:
Reducir los cólicos
Mejorar la regularidad de las heces
Menor riesgo de eczema
Apoyar el desarrollo inmunológico
Mejores cepas: Bifidobacterium infantis , B. breve , Lactobacillus reuteri DSM 17938.
Adultos
Apoya la estabilidad digestiva, la respuesta al estrés, la función metabólica y el equilibrio inmunológico.
Personas mayores
El envejecimiento se asocia con una reducción de la diversidad microbiana.
Los probióticos pueden ayudar:
Mejorar la regularidad
Apoyar la inmunidad
Reducir las infecciones
Mejorar la absorción de nutrientes
Cepas probióticas, dosis, seguridad y guía de suplementos

1. Comprensión de las cepas probióticas: una comparación a nivel profesional
Elegir probióticos por especie (por ejemplo, “Lactobacillus” o “Bifidobacterium”) es científicamente inadecuado.
La cepa determina el efecto, no sólo la especie.
A continuación se muestra una comparación de cepas de alto nivel que refleja la evidencia clínica actual.
1.1 Cepas de Lactobacillus
★ Lactobacillus rhamnosus GG (ATCC 53103)
Una de las cepas más estudiadas clínicamente del mundo.
Los beneficios incluyen:
Fuerte protección contra la diarrea asociada a antibióticos
Favorece la maduración del sistema inmunológico en los niños.
Reduce las infecciones respiratorias
Ayuda a regular el eje intestino-cerebro en condiciones relacionadas con el estrés.
Amplia seguridad en todos los grupos de edad
Los mecanismos implican la adhesión a las células epiteliales, la neutralización de toxinas y la mejora de IgA.
★ Lactobacillus plantarum 299v
Una cepa altamente resistente capaz de sobrevivir al ácido gástrico y adherirse a la mucosa intestinal.
Clínicamente demostrado que:
Reducir los síntomas del SII
Mejora la hinchazón y el dolor abdominal.
Favorecer la absorción de nutrientes
Mejorar la señalización antiinflamatoria
Ideal para formulaciones de salud digestiva.
★ Lactobacillus helveticus R0052
Una cepa psicobiótica utilizada en combinación con Bifidobacterium longum R0175.
Los beneficios incluyen:
niveles reducidos de cortisol
Menor estrés percibido
Mejora la regulación emocional
Mejor calidad del sueño
Este par es una de las combinaciones probióticas más investigadas para el bienestar mental.
1.2 Cepas de Bifidobacterium
★ Bifidobacterium infantis 35624
Una cepa clave para la modulación inmunitaria y la integridad de la barrera intestinal.
Excelente para:
SII (hinchazón, dolor abdominal, hipersensibilidad)
Síntomas digestivos provocados por la inflamación
Salud intestinal pediátrica
★ Bifidobacterium lactis BB-12
Una de las cepas de Bifidobacterium más documentadas del mundo.
La evidencia apoya:
Mejora la regularidad de las heces
Inmunidad mejorada
Riesgo reducido de infecciones respiratorias
Mejor estabilidad intestinal
★ Bifidobacterium longum NCC3001
Conocido por sus efectos sobre el eje intestino-cerebro.
Mostrado a:
Mejorar el procesamiento emocional
Reducir la hipersensibilidad visceral
Apoya el equilibrio del estrés y el estado de ánimo.
1.3 Cepas de Saccharomyces (levadura beneficiosa)
★ Saccharomyces boulardii CNCM I-745
Una levadura probiótica única con fuerte resistencia a los antibióticos.
Los usos admitidos incluyen:
Prevención de la diarrea asociada a antibióticos
Problemas digestivos relacionados con los viajes
Restauración del microbioma después de infecciones agudas
Apoyo durante la exposición a patógenos (p. ej., C. difficile )
Saccharomyces no coloniza el intestino sino que actúa durante su paso, lo que lo hace ideal para protocolos de protección a corto plazo.
2. Dosis: ¿Cuánta UFC necesitas realmente?
UFC (unidades formadoras de colonias) representa la cantidad de microorganismos viables en una dosis probiótica. Sin embargo, más no siempre es mejor.
Diferentes cepas requieren diferentes dosis clínicamente efectivas.
Pautas generales de dosificación:
| Objetivo | Rango típico de UFC |
|---|---|
| Mantenimiento intestinal diario | 1–10 mil millones de UFC |
| Síntomas digestivos leves | 10–20 mil millones de UFC |
| SII / enfermedades intestinales crónicas | 20–40+ mil millones de UFC |
| diarrea asociada a antibióticos | 10–20 mil millones de UFC (con S. boulardii ) |
| Apoyo inmunológico | 5–10 mil millones de UFC |
| Salud de la mujer (vaginal/urinaria) | 5–20 mil millones de UFC |
| Psicobióticos (estrés/estado de ánimo) | 1–3 mil millones de UFC por cepa |
| Niños | 1–5 mil millones de UFC |
Nota importante:
Un recuento elevado de UFC no compensa la mala calidad de la cepa ni la escasa capacidad de supervivencia.
La tensión importa más que el número.
3. Sistemas de administración de probióticos: por qué algunos funcionan mejor que otros
La supervivencia de los probióticos comienza antes de que el producto llegue al intestino.
La formulación debe proteger a los microorganismos de:
Calor
Humedad
Oxígeno
Ácido del estómago
Sales biliares
Estas son las tecnologías de entrega más comunes:
3.1 Cápsulas con recubrimiento entérico
Cápsulas con recubrimiento resistente al ácido que se disuelve únicamente en el intestino.
Ventajas:
Protege contra el ácido del estómago.
Garantiza una entrega dirigida
Ideal para cepas de Lactobacillus y Bifidobacterium.
3.2 Microencapsulación
Una tecnología más avanzada donde los organismos individuales se recubren con una capa protectora.
Beneficios:
Tasas de supervivencia más altas
Mejor estabilidad a temperatura ambiente
Mayor vida útil
Rendimiento mejorado en gomitas y bebidas.
3.3 Probióticos liofilizados vs. secados por calor
Liofilizado:
Más estable
Lo mejor para suplementos
Sobrevivir a temperatura ambiente
Secado al calor:
Más económico
Requiere refrigeración
Menos adecuado para la distribución global
Las marcas de alta calidad siempre eligen cepas liofilizadas.
3.4 Gomitas y formas líquidas
A los consumidores les encantan las gomitas, pero los probióticos en gomitas son técnicamente difíciles porque:
Las gomitas contienen humedad.
El calor durante la producción puede matar bacterias.
La viabilidad a largo plazo es más difícil de mantener
Dicho esto, la tecnología de microencapsulación ha mejorado significativamente la estabilidad de las gomitas.
Aun así, las gomitas suelen ofrecer menos UFC y menos opciones de cepas.
4. Seguridad, efectos secundarios y contraindicaciones
Los probióticos generalmente se consideran seguros para personas sanas.
Sin embargo, ciertos grupos necesitan una atención especial.
4.1 Efectos secundarios leves y comunes (generalmente temporales)
Gas
Hinchazón
Aumento de la frecuencia de las deposiciones
Malestar abdominal leve
Estos efectos generalmente desaparecen después de 3 a 7 días a medida que el microbioma se ajusta.
4.2 ¿Quién debe tener precaución?
Los probióticos pueden ser riesgosos para:
Pacientes inmunodeprimidos
Personas sometidas a quimioterapia
Personas con catéteres venosos centrales
Personas con pancreatitis grave
Pacientes con enfermedades críticas hospitalizados
Estos grupos sólo deben tomar probióticos bajo supervisión médica.
5. Cómo elegir un suplemento probiótico de alta calidad
La mayoría de los consumidores eligen los probióticos basándose en afirmaciones de marketing, lo que genera decepción. Una marca de suplementos seria o un usuario informado debería evaluar los probióticos según los siguientes criterios:

5.1 La etiqueta debe mostrar el nombre completo de la cepa
No solo Lactobacillus , no solo L. rhamnosus , sino la identificación de la cepa completa, por ejemplo:
L. rhamnosus GG
B. infantis 35624
S. boulardii CNCM I-745
Si falta la cepa, el producto no es un probiótico científicamente validado.
5,2 UFC garantizadas al vencimiento (no al momento de la fabricación)
Los probióticos de alta calidad especifican:
“X mil millones de UFC al vencimiento”.
Las marcas de mala calidad sólo garantizan UFC en la fecha de fabricación.
5.3 Tecnología de entrega
Elija probióticos con:
recubrimiento entérico
Microencapsulación
embalaje desecante
Evite productos con afirmaciones de estabilidad poco claras.
5.4 Pruebas de terceros
Los suplementos de primer nivel proporcionan:
Pureza microbiana
Pruebas de metales pesados
Detección de patógenos
Datos de vida útil
Los mercados internacionales a menudo requieren COA (Certificado de análisis).
5.5 Evite las fórmulas fáciles de usar
Algunas marcas añaden entre 20 y 30 cepas sin ninguna evidencia.
Más cepas ≠ mejores resultados.
Una fórmula bien estudiada de 3 a 6 cepas a menudo supera a una mezcla aleatoria de 20 cepas.
Prebióticos, simbióticos, interacciones dietéticas y ciencia del microbioma en el futuro
1. Probióticos vs. prebióticos vs. simbióticos: un análisis científico completo
Comprender las diferencias entre probióticos, prebióticos y simbióticos es esencial para diseñar fórmulas de suplementos eficaces y orientar las expectativas del consumidor. Aunque los tres suelen comercializarse juntos, desempeñan funciones biológicas completamente diferentes dentro del ecosistema intestinal.
1.1 ¿Qué son los prebióticos?
Los prebióticos son fibras y compuestos no digeribles que alimentan selectivamente a las bacterias beneficiosas del intestino. A diferencia de los probióticos, que son organismos vivos, los prebióticos son sustratos , lo que significa que actúan como fuente de alimento para los microbios beneficiosos.
Los ejemplos incluyen:
Fructooligosacáridos (FOS)
Galactooligosacáridos (GOS)
Inulina
Xilooligosacáridos (XOS)
almidón resistente
Ciertos polifenoles (por ejemplo, de bayas, té verde, cacao)
Los prebióticos mejoran la producción de ácidos grasos de cadena corta (AGCC), especialmente butirato , que está fuertemente vinculado con la regulación metabólica, la función de la barrera intestinal, el equilibrio inmunológico e incluso el rendimiento cognitivo.
Visión clave:
Los prebióticos actúan de forma lenta pero eficaz. Son la base que sustenta la salud del microbioma a largo plazo.
Sin la fibra adecuada, los suplementos probióticos no pueden funcionar de manera óptima, porque las bacterias beneficiosas carecen del combustible que necesitan para colonizar o influir en el entorno intestinal.
1.2 ¿Qué son los simbióticos?
Los simbióticos combinan probióticos + prebióticos en una sola formulación que mejora la supervivencia y la expresión de las cepas probióticas.
Hay dos tipos:
Simbióticos complementarios
Los prebióticos favorecen el crecimiento de una mayor variedad de bacterias beneficiosas, no necesariamente la cepa probiótica exacta del producto.
Ejemplo: L. plantarum + inulina.
Simbióticos sinérgicos
El prebiótico se selecciona específicamente para apoyar el crecimiento o la actividad metabólica de la cepa probiótica incluida.
Ejemplo: B. infantis + GOS (su sustrato preferido).
Los simbióticos pueden:
Mejorar el éxito de la colonización
Aumentar la producción de SCFA
Mejorar la regularidad de las heces
Mejorar la función inmunológica
Apoyar el equilibrio metabólico
Promover cambios más estables en el microbioma
Son especialmente valiosos para personas con baja ingesta de fibra dietética, uso frecuente de antibióticos o problemas digestivos crónicos.
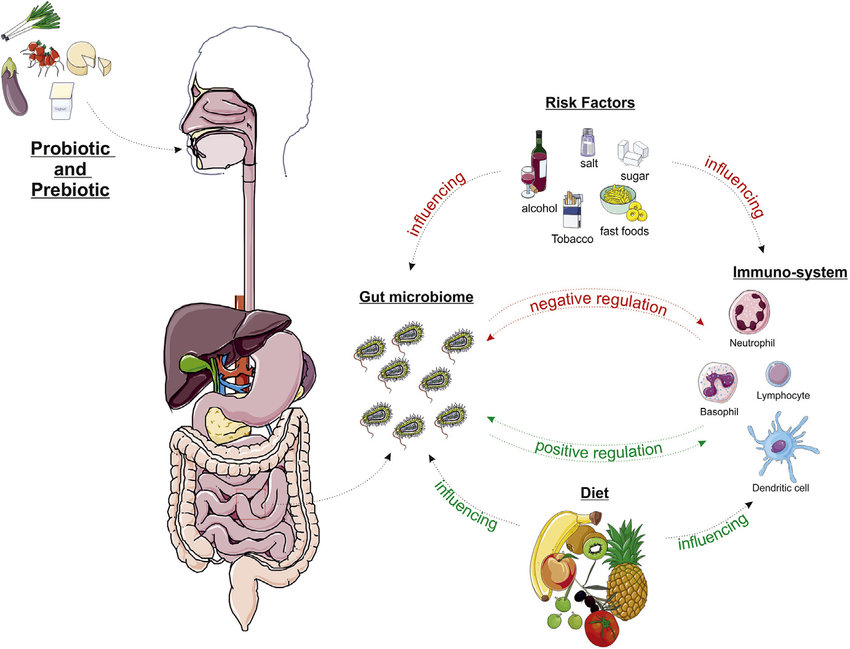
2. Cómo influye la dieta en la eficacia de los probióticos
Los probióticos no actúan de forma aislada. Su eficacia depende en gran medida del entorno alimentario del huésped. La dieta determina el sustrato en el que los probióticos intentan desarrollarse.
A continuación se presentan las interacciones dieta-microbioma más sólidas respaldadas por la investigación:
2.1 La ingesta de fibra es el determinante número uno de la diversidad del microbioma
Las poblaciones con dietas ricas en fibra (comunidades africanas tradicionales, seguidores de la dieta mediterránea) presentan:
Mayor diversidad microbiana
Mayor producción de SCFA
Tasas más bajas de enfermedades metabólicas
Mayor integridad de la barrera intestinal
Cuando la fibra dietética es insuficiente, las bacterias beneficiosas mueren de hambre, lo que produce disbiosis, incluso si alguien está tomando probióticos.
En otras palabras:
Un suplemento probiótico no puede solucionar una dieta baja en fibra.
Pero en un entorno rico en fibra, los probióticos prosperan y producen resultados significativamente mejores.
2.2 El alto contenido de azúcar y los alimentos procesados dañan el microbioma
Dietas altas en azúcar refinada y grasas procesadas:
Reducir las bacterias beneficiosas
Aumentar los microbios tolerantes a la bilis y vinculados a la inflamación
Interrumpir la señalización del eje intestino-cerebro
Promover el intestino permeable
Aumenta el riesgo de enfermedades relacionadas con la disbiosis
Incluso las mejores cepas probióticas no pueden contrarrestar de forma permanente la inflamación alimentaria si la dieta base sigue siendo altamente procesada.
2.3 Alimentos fermentados vs. suplementos probióticos
Los alimentos fermentados (yogur, kéfir, kimchi, kombucha, chucrut, miso, tempeh) contienen microbios vivos, pero:
Las cepas rara vez coinciden con las cepas probióticas clínicas.
Los recuentos de UFC varían drásticamente
Muchos microorganismos no pueden sobrevivir al ácido del estómago.
Los efectos son más leves y menos específicos.
Los alimentos fermentados favorecen la diversidad general del microbioma y la riqueza dietética, pero no reemplazan los suplementos probióticos clínicamente validados.
3. ¿Cuánto tardan en hacer efecto los probióticos? Un cronograma realista
Muchos consumidores esperan que los probióticos actúen en cuestión de días, pero el tiempo real depende de varios factores:
3.1 Efectos a corto plazo (0 a 2 semanas)
Los usuarios pueden experimentar:
Cambios digestivos leves (gases, cambios en los hábitos intestinales)
Mejora la regularidad de las heces
Reducción de la hinchazón
Mejor tolerancia a ciertos alimentos
Estos cambios reflejan interacciones y ajustes microbianos tempranos.
3.2 Efectos a medio plazo (3 a 6 semanas)
Los beneficios de los probióticos se hacen más notorios:
Reducción de los síntomas del SII
Menor frecuencia de brotes digestivos
Mayor resiliencia inmunológica
Mejora la estabilidad del microbioma vaginal
Mejor estabilidad del estado de ánimo y respuesta al estrés.
Esta fase refleja una colonización estabilizada y una modulación inmune.
3.3 Efectos a largo plazo (2 a 6 meses)
Cambios profundos impulsados por el microbioma:
Mayor diversidad microbiana
Barrera intestinal más fuerte
Marcadores metabólicos mejorados
Inflamación sistémica reducida
Bienestar mental y emocional más estable
Mejoras duraderas en la digestión.
Estos efectos requieren constancia y patrones dietéticos de apoyo.
4. Futuras direcciones en la ciencia de los probióticos y el microbioma
El campo de los probióticos está evolucionando rápidamente. La próxima década traerá avances revolucionarios que irán mucho más allá de la generación actual de suplementos.
4.1 Probióticos de precisión (personalización a nivel de cepa)
La secuenciación genómica permite a los investigadores identificar cepas altamente específicas adaptadas a los perfiles de microbioma individuales. Los probióticos futuros serán personalizados , en lugar de universales.
4.2 Postbióticos: La próxima generación de terapias microbianas
Los postbióticos son productos microbianos no vivos , incluidos metabolitos, enzimas, péptidos y fragmentos de células.
Ofrecen ventajas:
No hay problemas de supervivencia
Altamente estable
Mecanismos claros
Fuertes efectos inmunomoduladores
Los postbióticos podrían pronto superar a los probióticos tradicionales en ciertos usos terapéuticos.
4.3 Bioterapéuticos vivos (LBP)
Los LBP son microbios de grado farmacéutico diseñados como medicamentos regulados , no suplementos.
Se dirigen a condiciones como:
Colitis ulcerosa
enfermedad de Crohn
Infecciones resistentes a los antibióticos
Trastornos metabólicos
Este campo redefinirá cómo utilizamos los microorganismos para la terapia médica.
4.4 Terapias cognitivas y del estado de ánimo basadas en el microbioma
La “psicobiótica” se expandirá a:
Apoyo para la ansiedad y la depresión
Optimización del sueño
Mejora del rendimiento cognitivo
Manejo de enfermedades neuroinflamatorias
Las primeras investigaciones son muy prometedoras.
4.5 Investigación sobre el microbioma y la longevidad
Estudios emergentes sugieren que el microbioma influye en:
Tasa de envejecimiento
Mantenimiento muscular
Equilibrio hormonal
Inflamación (“inflammaging”)
Enfermedades relacionadas con la edad
Los probióticos del futuro podrían convertirse en componentes centrales de las estrategias antienvejecimiento.
5. Resumen final: Qué ofrecen realmente los probióticos
Los probióticos no son píldoras mágicas, pero cuando se eligen adecuadamente, se complementan con la dieta y se toman de manera constante, brindan profundos beneficios respaldados por décadas de investigación científica.
Una estrategia probiótica verdaderamente de alta calidad implica:
Especificidad de la cepa
UFC adecuadas
Potente tecnología de entrega
Apoyo prebiótico
Selección personalizada
Consistencia a largo plazo
Expectativas basadas en evidencia
El microbioma se encuentra en el centro de la salud humana: bienestar digestivo, inmunológico, metabólico, mental e incluso de la piel. Apoyarlo con probióticos específicos es una de las formas más poderosas, respaldadas por la ciencia, de mejorar la salud a largo plazo.
Lista de referencias
1. Directrices de la FAO/OMS sobre probióticos
FAO/OMS. (2002). Directrices para la evaluación de probióticos en los alimentos .
https://www.fao.org/3/a0512e/a0512e.pdf
2. NIH – Centro Nacional de Salud Complementaria e Integral (NCCIH)
Probióticos: lo que necesitas saber
https://www.nccih.nih.gov/health/probiotics-what-you-need-to-know
3. ISAPP – Asociación Científica Internacional de Probióticos y Prebióticos
Declaraciones de consenso y recursos científicos
https://isappscience.org
4. Lactobacillus rhamnosus GG (ATCC 53103)
Szajewska H. et al., The Lancet Infectious Diseases , 2015.
Índice PubMed: https://pubmed.ncbi.nlm.nih.gov/25547277/
5. Lactobacillus plantarum 299v – Investigación sobre el SII
Johansson ML et al. Estudio clínico sobre el SII.
Búsqueda en PubMed: https://pubmed.ncbi.nlm.nih.gov/?term=Lactobacillus+plantarum+299v
6. Bifidobacterium infantis 35624
Whorwell PJ et al., Gastroenterología , 2006.
https://pubmed.ncbi.nlm.nih.gov/16401471/
7. Saccharomyces boulardii CNCM I-745
McFarland LV, Avances terapéuticos en gastroenterología .
https://pubmed.ncbi.nlm.nih.gov/?term=Saccharomyces+boulardii+CNCM+I-745
8. Psicobióticos: L. helveticus R0052 y B. longum R0175
Messaoudi M. et al., Revista Británica de Nutrición , 2011.
https://pubmed.ncbi.nlm.nih.gov/21736802/
9. Investigación del eje intestino-cerebro – Cryan & Dinan
Estudios fundamentales:
https://pubmed.ncbi.nlm.nih.gov/?term=Microbioma de Cryan y Dinan
10. Investigación sobre probióticos infantiles (B. infantis)
Centro de Investigación sobre Leche Humana y Lactancia de UC Davis
https://hmnb.ucdavis.edu
11. Lactobacillus reuteri DSM 17938 para el cólico infantil
https://pubmed.ncbi.nlm.nih.gov/?term=Lactobacillus+reuteri+DSM+17938
12. Salud de la mujer: cepas GR-1 y RC-14
Reid G. et al., Revista de enfermedades infecciosas .
https://pubmed.ncbi.nlm.nih.gov/?term=Reid+GR-1+RC-14
13. Salud metabólica – Lactobacillus gasseri SBT2055
https://pubmed.ncbi.nlm.nih.gov/?term=Lactobacillus+gasseri+SBT2055
14. Bifidobacterium breve B-3
https://pubmed.ncbi.nlm.nih.gov/?term=Bifidobacterium+breve+B-3
15. Investigación sobre la barrera intestinal y los AGCC
https://pubmed.ncbi.nlm.nih.gov/?term=SCFA+gut+barrier
16. EFSA (Autoridad Europea de Seguridad Alimentaria)
Lista de presunción calificada de seguridad
https://www.efsa.europa.eu
17. Avisos GRAS de la FDA para ingredientes probióticos
https://www.fda.gov/food/generally-recognized-safe-gras
18. ClinicalTrials.gov – Ensayos clínicos de probióticos
https://clinicaltrials.gov
19. PubMed – Búsqueda en la base de datos general de probióticos
https://pubmed.ncbi.nlm.nih.gov/?term=probióticos






