1. Que sont les probiotiques ? Définition scientifique au niveau de la souche
Bien que le terme « probiotiques » soit devenu très courant dans les produits de consommation, sa définition scientifique est bien plus précise et restrictive que la plupart des gens ne le pensent. Selon la FAO/OMS, les probiotiques sont des micro-organismes vivants qui, administrés en quantités adéquates, confèrent un bénéfice pour la santé de l’hôte . Chaque élément de cette définition repose sur des bases scientifiques solides.
Les probiotiques doivent être vivants au moment de leur consommation . Cela paraît évident, mais de nombreux produits commerciaux ne garantissent pas leur survie lors de la fabrication, du transport et du stockage. L'activité biologique d'un probiotique dépend de sa capacité à résister aux conditions difficiles de l'estomac – notamment l'acidité gastrique, les sels biliaires et les enzymes digestives – avant d'atteindre l'intestin vivant. Les bactéries mortes ou les fragments postbiotiques peuvent encore avoir certains effets physiologiques, mais ils ne peuvent être considérés comme des probiotiques au sens strict.
Les probiotiques doivent être pris à doses adéquates , généralement mesurées en UFC (unités formant colonies). Différentes souches requièrent différents seuils minimaux pour produire des effets mesurables. Un produit vantant « des millions de bactéries vivantes » est pratiquement inutile ; des effets cliniques significatifs sont généralement observés à partir de milliards de bactéries .
Et surtout, les probiotiques doivent être définis au niveau de la souche . Cela signifie que leur nom scientifique complet doit inclure le genre, l'espèce et un code alphanumérique de souche. Par exemple :
Lactobacillus rhamnosus = espèce
Lactobacillus rhamnosus GG (ATCC 53103) = souche spécifique aux bienfaits prouvés
Deux organismes peuvent appartenir au même genre et à la même espèce, mais se comporter comme des entités biologiques totalement différentes s'ils possèdent des identifiants de souche différents. C'est pourquoi des affirmations telles que « Lactobacillus améliore la digestion » sont scientifiquement dénuées de sens. Seules des preuves spécifiques à la souche peuvent établir un réel bénéfice pour la santé.
En clair : le numéro de souche est ce qui distingue un probiotique scientifiquement validé d’une simple bactérie quelconque.
Ce niveau de précision est ce qui distingue les compléments probiotiques de haute qualité des produits vagues à base de « cultures vivantes » ou des aliments fermentés qui ne font pas l'objet de tests cliniques contrôlés.
2. Le microbiome humain : l’écosystème et le soutien des probiotiques
Pour comprendre l’action des probiotiques, il est essentiel de comprendre le système avec lequel ils interagissent : le microbiome humain . L’intestin humain abrite à lui seul des milliards de micro-organismes — bactéries, champignons, virus et archées — formant une communauté écologique complexe, bien plus vaste que le nombre de cellules de l’organisme. Cet écosystème est dynamique, diversifié et profondément intégré à la physiologie humaine.
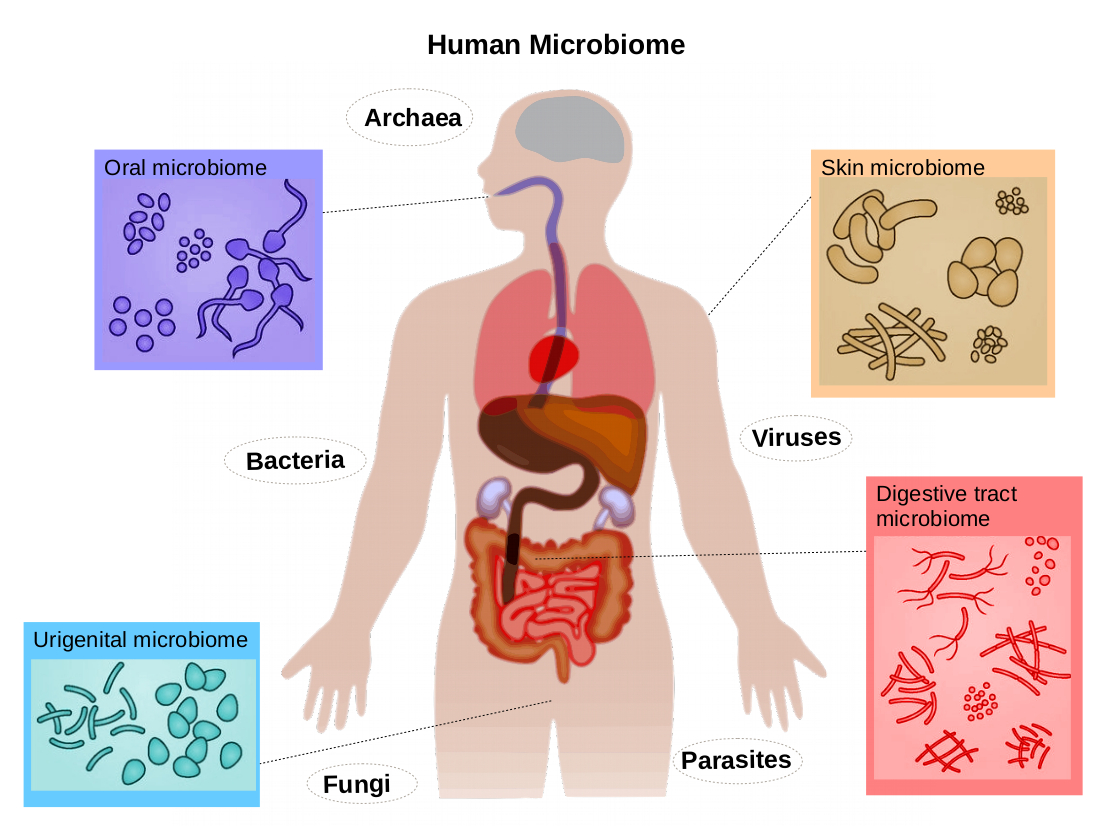
Le microbiome intestinal participe à des centaines de fonctions essentielles :
Digérer les fibres alimentaires que les enzymes humaines ne peuvent pas décomposer
Production d'acides gras à chaîne courte (AGCC) qui nourrissent les cellules du côlon
Synthétiser des vitamines telles que la vitamine K et certaines vitamines B
Entraîner le système immunitaire à distinguer les menaces des stimuli inoffensifs
Réguler l'inflammation dans tout le corps
Communiquer avec le cerveau par le biais de signaux neuronaux, hormonaux et biochimiques
Influence sur le métabolisme , la glycémie, les taux de lipides et le stockage des graisses
Un écosystème intestinal sain est comparable à une forêt luxuriante : riche en biodiversité, équilibré et résilient. Or, les modes de vie modernes peuvent facilement perturber cet équilibre. Une alimentation riche en aliments ultra-transformés, le stress chronique, un sommeil de mauvaise qualité, la prise d’antibiotiques, la consommation d’alcool ou les infections gastro-intestinales peuvent tous provoquer une dysbiose , c’est-à-dire un déséquilibre de la composition microbienne.
La dysbiose n'est pas un problème mineur ; elle est désormais associée à :
Syndrome du côlon irritable (SCI)
maladies inflammatoires de l'intestin
Obésité et syndrome métabolique
Anxiété, dépression et changements cognitifs
Problèmes de peau tels que l'eczéma, l'acné et la rosacée
Allergies et réactions auto-immunes
Dans ce contexte, les probiotiques ne sont pas considérés comme des solutions miracles, mais comme des outils biologiques conçus pour contribuer à rétablir l'équilibre écologique . Ils ne peuvent pas tout résoudre à eux seuls, mais, correctement sélectionnés, ils influencent cet environnement complexe de manière à favoriser significativement la santé humaine.
3. Comment fonctionnent les probiotiques : mécanismes détaillés
La plupart des articles de base résument les mécanismes des probiotiques en une seule phrase : « Les probiotiques aident à rétablir l'équilibre intestinal et à soutenir l'immunité. »
Cette explication est tellement simplifiée qu'elle en devient trompeuse. Vous trouverez ci-dessous une analyse détaillée, mécanisme par mécanisme , rédigée dans le style d'un concepteur de formules, et non d'un consommateur lambda.
Exclusion concurrentielle — Les probiotiques occupent l’« espace » avant les agents pathogènes
Dans l'intestin, les microbes se disputent l'espace sur la muqueuse intestinale. Cette surface étant limitée, les organismes qui s'y fixent en premier prennent l'avantage. Certaines souches probiotiques possèdent des protéines d'adhésion spécifiques qui leur permettent de s'ancrer plus efficacement que les bactéries pathogènes.
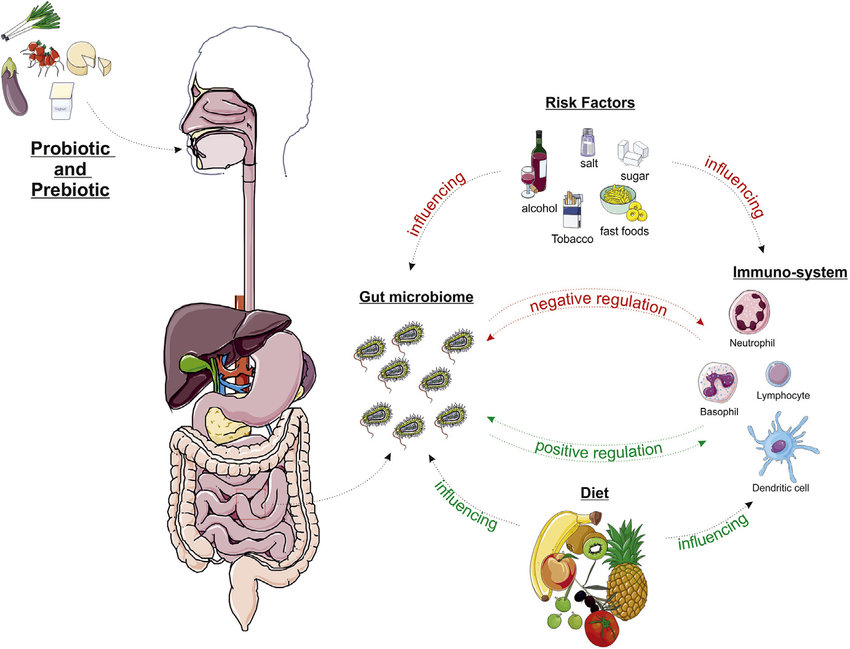
En occupant ces sites de fixation, les probiotiques empêchent les espèces pathogènes d’établir des colonies, un phénomène connu sous le nom d’exclusion compétitive .
Pourquoi c'est important :
Réduit la prolifération pathogène
Protège contre les troubles post-antibiotiques
Réduit les épisodes de diarrhée ou les troubles digestifs du voyageur
Ce mécanisme est particulièrement important immédiatement après un traitement antibiotique, lorsque le « terrain » microbien est largement disponible pour la recolonisation.
Production d'acides organiques — Création d'un environnement hostile aux mauvaises bactéries
De nombreuses souches de Lactobacillus et de Bifidobacterium fermentent les glucides pour produire de l'acide lactique , de l'acide acétique et d'autres métabolites qui abaissent le pH du milieu intestinal.
Les bactéries pathogènes, telles que E. coli , Clostridium et Salmonella , préfèrent un environnement plus alcalin ; un intestin légèrement acide limite donc leur prolifération.
Cette acidification :
Améliore l'absorption des nutriments
Améliore la solubilité des minéraux
Limite la croissance des microbes nuisibles
Favorise une succession microbienne plus saine
En pratique, cela signifie que les probiotiques ne « tuent » pas les bactéries nocives comme le font les antibiotiques ; ils les supplantent et les affament en modifiant l’environnement.
Modulation immunitaire — Les probiotiques ne renforcent pas l’immunité ; ils l’équilibrent.
L'intestin est le plus grand organe immunitaire du corps humain. Environ 70 % des cellules immunitaires se trouvent dans le tube digestif. Les probiotiques interagissent avec les cellules immunitaires par le biais de récepteurs de reconnaissance de motifs, de la signalisation des cytokines et de métabolites moléculaires.
Mais les probiotiques ne se contentent pas de « renforcer l’immunité ».
Ils agissent comme modulateurs immunitaires , ce qui signifie :
Renforcer l'immunité déficiente
Calmer les réactions inflammatoires excessives
Amélioration de la sécrétion d'IgA à la surface de la muqueuse
Ajustement précis des réponses des lymphocytes T pour réduire l'hypersensibilité
Ce double effet explique pourquoi les probiotiques sont utiles dans des situations qui semblent contradictoires :
Renforcer la résistance aux infections
Soulager les symptômes de l'eczéma et des allergies
Maintenir l’équilibre immunitaire en période de stress
Tout cela fait partie du même mécanisme de régulation — et non d'un effet contradictoire.
Renforcer la barrière intestinale — Se protéger contre l’hyperperméabilité intestinale
La barrière intestinale est maintenue par des protéines appelées jonctions serrées , qui régulent le passage des substances dans la circulation sanguine. Lorsque cette barrière s'affaiblit (en raison du stress, des toxines, de l'inflammation, d'une mauvaise alimentation ou de la consommation d'alcool), des particules qui devraient rester dans l'intestin passent dans la circulation sanguine. Ceci déclenche une inflammation chronique de bas grade, souvent appelée endotoxémie métabolique .
Il a été démontré que certaines souches probiotiques :
Augmenter l'expression des protéines des jonctions serrées
Stimuler la production de mucine
Favoriser la régénération épithéliale
Réduire la perméabilité (« intestin perméable »)
Une barrière intestinale plus saine améliore non seulement la digestion, mais réduit également l'inflammation systémique, ce qui a un impact sur la santé de la peau, la stabilité métabolique et même l'humeur.
Améliorer la production d'AGCC — Un carburant pour les cellules du côlon et la santé à long terme
Les acides gras à chaîne courte (AGCC), notamment le butyrate , sont produits lorsque les bactéries intestinales fermentent les fibres et les prébiotiques. Butyrate :
La principale source d'énergie des cellules du côlon
Réduit l'inflammation
Améliore la fonction métabolique
Favorise la sensibilité à l'insuline
Affecte la synthèse des neurotransmetteurs
Contribue à réguler l'appétit et la satiété
Les probiotiques agissent souvent en synergie avec les fibres alimentaires :
Ils contribuent à une fermentation plus efficace des fibres, augmentant ainsi le rendement en acides gras à chaîne courte (AGCC). C'est l'une des raisons pour lesquelles les symbiotiques (probiotiques + prébiotiques) sont souvent plus efficaces que les probiotiques seuls.
Axe intestin-cerveau : comment les microbes influencent l’humeur, le stress et le sommeil
L'intestin produit environ 90 % de la sérotonine de l'organisme , et les métabolites microbiens influencent les voies de neurotransmission, le nerf vague et les canaux inflammatoires – trois des facteurs les plus importants de la santé mentale et émotionnelle.
Il a été démontré que certaines souches (par exemple, Lactobacillus helveticus R0052 et Bifidobacterium longum R0175) :
Réduire le cortisol
Améliorer la résilience au stress
Favoriser la qualité du sommeil
Influencer le traitement émotionnel
Ce domaine de recherche est connu sous le nom de psychobiotique , l'un des domaines qui se développe le plus rapidement dans le domaine des sciences du microbiome.
Régulation métabolique — Le lien microbien avec le poids et la glycémie
Les probiotiques influencent indirectement le métabolisme par le biais de :
Réduire la perméabilité intestinale → moins d'inflammation
Modulation des hormones comme le GLP-1
Influant sur l'efficacité de l'absorption des graisses
Régulation du métabolisme des acides biliaires
Influence sur le rapport Firmicutes/Bacteroidetes
Les probiotiques, à eux seuls, n'entraînent pas une perte de poids spectaculaire, mais ils contribuent à un environnement métabolique qui favorise :
Meilleur contrôle de la glycémie
Réduction de l'inflammation
Accumulation de graisse viscérale inférieure
Bienfaits cliniques des probiotiques
Les probiotiques influencent la santé humaine à travers un large éventail de systèmes physiologiques. Leurs effets sont très spécifiques à chaque souche , ce qui signifie que chaque souche possède des mécanismes d'action, des preuves cliniques et une valeur thérapeutique différents. Vous trouverez ci-dessous une analyse détaillée, catégorie par catégorie, des bienfaits des probiotiques, rédigée avec un niveau de détail médical et des informations pratiques pertinentes pour les marques de compléments alimentaires et les consommateurs.
1. Santé digestive : le bienfait le plus établi et le plus étudié
La santé digestive demeure l'application des probiotiques la plus validée scientifiquement, car le microbiote intestinal influence directement la motilité, l'absorption des nutriments, l'activité immunitaire et l'intégrité de la muqueuse. La dysbiose, souvent causée par les antibiotiques, le stress, une mauvaise alimentation, une infection ou une inflammation chronique, peut se manifester par de la constipation, de la diarrhée, des ballonnements, des douleurs abdominales ou des troubles du transit intestinal.
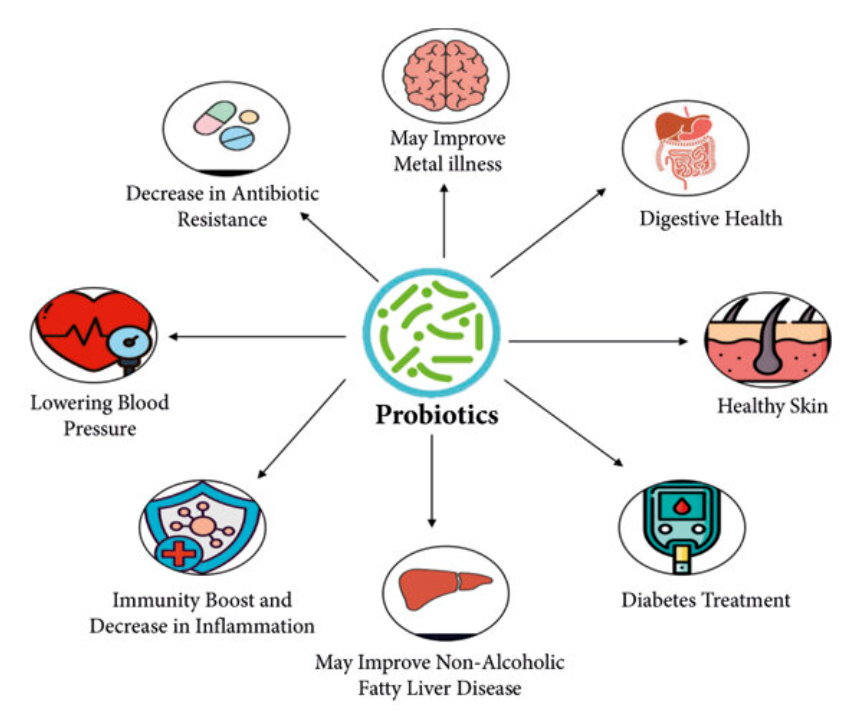
Les probiotiques favorisent la stabilité digestive par plusieurs mécanismes : régulation de la motilité, déplacement des microbes producteurs de gaz, renforcement des barrières muqueuses, réduction de l’inflammation et restauration de la diversité microbienne.
1.1 Syndrome du côlon irritable (SCI)
Le syndrome de l'intestin irritable (SII) touche des millions de personnes dans le monde et implique une interaction complexe entre hypersensibilité viscérale, activation immunitaire, dysbiose et stress.
Plusieurs essais contrôlés randomisés démontrent que certaines souches peuvent améliorer les symptômes du syndrome de l'intestin irritable en :
réduire les douleurs abdominales
améliorer la régularité intestinale
réduire les ballonnements
modulation des biomarqueurs inflammatoires
Les souches les plus étudiées comprennent :
Lactobacillus plantarum 299v – améliore les douleurs abdominales et la tolérance aux gaz
Bifidobacterium infantis 35624 – réduit les ballonnements, les douleurs et les irrégularités intestinales
Saccharomyces boulardii CNCM I-745 – réduit les symptômes du syndrome de l'intestin irritable à prédominance de diarrhée
Ces souches agissent par le biais d'une activité anti-inflammatoire, d'une augmentation des acides gras à chaîne courte et d'une modulation immunitaire de l'hôte.
1.2 Constipation (constipation fonctionnelle et transit lent)
La constipation résulte fréquemment d'une production insuffisante d'AGCC, d'une motilité intestinale altérée ou d'une diversité microbienne réduite.
Les probiotiques peuvent stimuler le péristaltisme en produisant des métabolites qui interagissent avec le système nerveux entérique.
Souches présentant des preuves solides :
Bifidobacterium lactis BB-12 – augmente la fréquence des selles et améliore leur aspect.
Lactobacillus casei Shirota – améliore la motilité et réduit le temps de transit intestinal
Lactobacillus rhamnosus GG – bénéfique pour les adultes et les enfants
Les probiotiques agissent souvent en synergie avec les prébiotiques (FOS, inuline) pour améliorer les habitudes intestinales.
1.3 Diarrhée, y compris la diarrhée associée aux antibiotiques (DAA)
L'une des utilisations cliniques les plus prouvées des probiotiques est la prévention de la diarrhée associée aux antibiotiques (DAA), où les antibiotiques perturbent la flore intestinale normale et permettent la prolifération d'agents pathogènes opportunistes.
Les souches les plus étudiées comprennent :
Saccharomyces boulardii CNCM I-745 – référence en matière de prévention de la diarrhée associée aux antibiotiques
Lactobacillus rhamnosus GG – réduit l'incidence et la durée
Bifidobacterium breve, souche Yakult – stabilise l’équilibre microbien pendant un traitement antibiotique
Ces souches présentent des activités d'inhibition des agents pathogènes, de normalisation de la signalisation immunitaire et de neutralisation des toxines.
1.4 Ballonnements, gaz et dyspepsie
La production de gaz et la distension abdominale résultent souvent de déséquilibres de fermentation ou de modifications transitoires du microbiote.
Souches utiles :
Lactobacillus plantarum 299v
Bifidobacterium longum NCC3001 – réduit l’hypersensibilité viscérale
Lactobacillus acidophilus NCFM
Ces souches améliorent la tolérance aux gaz, réduisent le stress de fermentation et améliorent la résilience de la muqueuse.
2. Soutien immunitaire : équilibrer, et non « booster » l’immunité
Le système immunitaire et le microbiote intestinal interagissent constamment. Les probiotiques influencent l'immunité en modulant les voies inflammatoires, en améliorant la défense humorale des muqueuses et en stabilisant la signalisation immunitaire intestinale. Plutôt que de « renforcer l'immunité » de manière indiscriminée, les probiotiques optimisent la réponse immunitaire , réduisant l'inflammation excessive tout en renforçant la résistance aux agents pathogènes.
Les principaux bienfaits pour le système immunitaire comprennent :
Réduction de la fréquence et de la gravité des rhumes
Amélioration de la sécrétion d'IgA muqueuse
Moins d'inflammation dans le tube digestif
Rétablissement plus rapide après une infection
Réponse vaccinale accrue dans certaines populations
Souches avec preuves :
Lactobacillus paracasei CASEI 431 – améliore la réponse immunitaire aux vaccins
Bifidobacterium animalis BB-12 – renforce l’immunité muqueuse
Lactobacillus rhamnosus GG – réduit les infections respiratoires chez l'enfant
Lactobacillus casei Shirota – module l'activité des cellules NK
Ces souches ne stimulent pas le système immunitaire de manière agressive ; elles le guident vers l'équilibre, réduisant ainsi la suractivation inutile tout en renforçant les défenses de première ligne.
3. Santé des femmes : Microbiome vaginal et soutien des voies urinaires
Le microbiote vaginal féminin est dominé par les lactobacilles, qui maintiennent un environnement acide (pH optimal ≈ 4,5) grâce à la production d'acide lactique. Le stress, les changements hormonaux, les antibiotiques et l'activité sexuelle peuvent perturber cet écosystème, augmentant ainsi le risque de vaginose bactérienne, de mycoses vaginales et d'inconfort urinaire.
Les probiotiques contribuent à la santé des femmes en :
Rétablir la dominance des lactobacilles
Diminution du pH vaginal
Production de peroxyde d'hydrogène pour inhiber les agents pathogènes
Renforcement des barrières muqueuses
Réduire la récurrence de la vaginose bactérienne (VB)
Souches cliniquement significatives :
Lactobacillus crispatus CTV-05 – la référence en matière de restauration du microbiome vaginal
Lactobacillus rhamnosus GR-1 + Lactobacillus reuteri RC-14 – une paire synergique largement validée dans les études
Lactobacillus jensenii – favorise l’intégrité de la muqueuse
Ces souches peuvent être prises par voie orale ou administrées par voie intravaginale selon le contexte clinique.
4. Santé de la peau : l’axe intestin-peau
La peau et l'intestin entretiennent des liens immunologiques et métaboliques étroits. Une dysbiose peut accroître l'inflammation systémique, fragiliser la barrière épithéliale et favoriser des affections telles que l'acné, l'eczéma et les rougeurs.
Les probiotiques peuvent être bénéfiques pour la peau en :
Réduction des cytokines inflammatoires
Soutien de l'intégrité de la barrière intestinale
Modulation de la production de sébum
Équilibrer les métabolites microbiens associés aux poussées cutanées
Améliorer la rétention d'hydratation de la peau
Souches impliquées dans les bienfaits pour la peau :
Lactobacillus rhamnosus GG – réduit le risque d'eczéma chez les nourrissons et les enfants
Bifidobacterium longum – diminue la sensibilité et l'inflammation
Lactobacillus paracasei ST11 – contribue à la barrière cutanée et à l'hydratation
Bien que les probiotiques ne soient pas une solution miracle, ils favorisent l'équilibre interne qui se reflète sur la santé de la peau.
5. L’axe intestin-cerveau : les probiotiques pour l’humeur, le stress et les fonctions cognitives
L'un des domaines les plus passionnants et évolutifs de la recherche sur les probiotiques est l' axe microbiote-intestin-cerveau , un réseau de communication impliquant le nerf vague, les neurotransmetteurs, la signalisation immunitaire et les métabolites microbiens.
La dysbiose est désormais reconnue comme un facteur contribuant à :
Anxiété
sensibilité au stress
Mauvais sommeil
Brouillard cognitif
Symptômes dépressifs légers
Les souches psychobiotiques ayant fait l'objet de preuves comprennent :
Lactobacillus helveticus R0052 + Bifidobacterium longum R0175 – réduisent le cortisol et améliorent la réponse au stress
Bifidobacterium longum NCC3001 – améliore le traitement émotionnel
Lactobacillus plantarum PS128 – preuves émergentes de régulation de l’humeur
Ces souches influencent les voies de la sérotonine, la signalisation GABAergique, l'inflammation et le nerf vague.
6. Les probiotiques pour la santé métabolique et la gestion du poids
Bien que les probiotiques ne soient pas des médicaments pour la perte de poids, ils influent sur la régulation métabolique par plusieurs voies :
Réduction de la perméabilité intestinale (diminution de l'inflammation systémique)
Modulation des hormones GLP-1 et de l'appétit
Influence sur le métabolisme des triglycérides
Influence sur le stockage des graisses et la dépense énergétique
Favoriser un meilleur contrôle de la glycémie
Souches importantes :
Lactobacillus gasseri SBT2055 – associé à une réduction de la graisse viscérale
Bifidobacterium breve B-3 – lié à une meilleure composition corporelle
Les souches de Lactobacillus plantarum favorisent l'équilibre métabolique.
Ces effets sont modestes mais significatifs lorsqu'ils sont associés à des interventions sur l'alimentation et le mode de vie.
7. Les probiotiques à tous les âges : nourrissons, adultes et personnes âgées
nourrissons
Les 1000 premiers jours de la vie sont cruciaux pour la formation du microbiome.
Les probiotiques peuvent aider :
Réduire les coliques
Améliorer la régularité des selles
risque d'eczéma réduit
Soutenir le développement immunitaire
Meilleures souches : Bifidobacterium infantis , B. breve , Lactobacillus reuteri DSM 17938.
Adultes
Favorise la stabilité digestive, la réponse au stress, la fonction métabolique et l'équilibre immunitaire.
Les aînés
Le vieillissement est associé à une réduction de la diversité microbienne.
Les probiotiques peuvent aider :
Améliorer la régularité
Soutien de l'immunité
Réduire les infections
Améliorer l'absorption des nutriments
Souches probiotiques, dosage, sécurité et guide des suppléments

1. Comprendre les souches probiotiques : une comparaison de niveau professionnel
Choisir les probiotiques en fonction de l'espèce (par exemple, « Lactobacillus » ou « Bifidobacterium ») est scientifiquement inadéquat.
C’est la souche qui détermine l’effet, et non l’espèce seule.
Vous trouverez ci-dessous une comparaison de souches de haut niveau qui reflète les données cliniques actuelles.
1.1 Souches de Lactobacillus
★ Lactobacillus rhamnosus GG (ATCC 53103)
L'une des souches les plus étudiées cliniquement au monde.
Les avantages comprennent :
Protection efficace contre la diarrhée associée aux antibiotiques
Favorise la maturation du système immunitaire chez l'enfant
Réduit les infections respiratoires
Contribue à réguler l'axe intestin-cerveau dans les conditions liées au stress
La sécurité générale concerne tous les groupes d'âge.
Les mécanismes impliquent l'adhésion aux cellules épithéliales, la neutralisation des toxines et l'amplification des IgA.
★ Lactobacillus plantarum 299v
Une souche très résistante, capable de survivre à l'acide gastrique et d'adhérer à la muqueuse intestinale.
Cliniquement démontré :
Réduire les symptômes du syndrome du côlon irritable
Améliorer les ballonnements et les douleurs abdominales
Favoriser l'absorption des nutriments
Renforcer la signalisation anti-inflammatoire
Idéal pour les préparations favorisant la santé digestive.
★ Lactobacillus helveticus R0052
Une souche psychobiotique utilisée en combinaison avec Bifidobacterium longum R0175.
Les avantages comprennent :
Réduction des niveaux de cortisol
Réduction du stress perçu
Amélioration de la régulation émotionnelle
Meilleure qualité du sommeil
Ce duo est l'une des combinaisons probiotiques les plus étudiées pour le bien-être mental.
1.2 Souches de Bifidobacterium
★ Bifidobactérie infantis 35624
Une souche clé pour la modulation immunitaire et l'intégrité de la barrière intestinale.
Idéal pour :
Syndrome du côlon irritable (ballonnements, douleurs abdominales, hypersensibilité)
Symptômes digestifs liés à l'inflammation
Santé intestinale pédiatrique
★ Bifidobacterium lactis BB-12
L'une des souches de Bifidobacterium les plus documentées au monde.
Les preuves soutiennent :
Amélioration de la régularité des selles
Immunité renforcée
Risque réduit d'infections respiratoires
Meilleure stabilité intestinale
★ Bifidobactérie longum NCC3001
Connu pour ses effets sur l'axe intestin-cerveau.
Présenté à :
Améliorer le traitement émotionnel
Réduire l'hypersensibilité viscérale
Favoriser l'équilibre du stress et de l'humeur
1.3 Souches de Saccharomyces (levures bénéfiques)
★ Saccharomyces boulardii CNCM I-745
Une levure probiotique unique, dotée d'une forte résistance aux antibiotiques.
Les utilisations prises en charge incluent :
Prévention de la diarrhée associée aux antibiotiques
Troubles digestifs liés aux voyages
Restauration du microbiome après des infections aiguës
Soutien lors d'une exposition à un agent pathogène (par exemple, C. difficile )
Saccharomyces ne colonise pas l'intestin mais agit lors de son passage, ce qui le rend idéal pour les protocoles de protection à court terme.
2. Dosage : De combien d'UFC avez-vous réellement besoin ?
Les UFC (unités formant colonies) représentent le nombre de micro-organismes viables dans une dose de probiotiques. Mais plus n'est pas toujours mieux.
Différentes souches nécessitent différentes doses cliniquement efficaces.
Recommandations générales de dosage :
| But | Plage typique d'UFC |
|---|---|
| entretien quotidien de l'intestin | 1 à 10 milliards d'UFC |
| Symptômes digestifs légers | 10 à 20 milliards d'UFC |
| Syndrome du côlon irritable / affections intestinales chroniques | 20 à plus de 40 milliards d'UFC |
| Diarrhée associée aux antibiotiques | 10 à 20 milliards d'UFC (avec S. boulardii ) |
| Soutien immunitaire | 5 à 10 milliards d'UFC |
| Santé des femmes (vaginale/urinaire) | 5 à 20 milliards d'UFC |
| Psychobiotiques (stress/humeur) | 1 à 3 milliards d'UFC par souche |
| Enfants | 1 à 5 milliards d'UFC |
Note importante :
Un nombre élevé d'UFC ne compense pas une faible qualité de la souche ou une faible capacité de survie.
La souche importe plus que le nombre.
3. Systèmes d'administration de probiotiques : pourquoi certains fonctionnent mieux que d'autres
La survie des probiotiques commence avant même que le produit n'atteigne votre intestin.
La formulation doit protéger les micro-organismes contre :
Chaleur
Humidité
Oxygène
Acide gastrique
sels biliaires
Voici les technologies de diffusion les plus courantes :
3.1 Capsules à enrobage entérique
Capsules à enrobage résistant à l'acide qui se dissolvent uniquement dans les intestins.
Avantages :
Protège contre l'acidité gastrique
Garantit une livraison ciblée
Idéal pour les souches de Lactobacillus et de Bifidobacterium
3.2 Microencapsulation
Une technologie plus avancée où les organismes individuels sont recouverts d'une couche protectrice.
Avantages:
Des taux de survie plus élevés
Meilleure stabilité à température ambiante
Durée de conservation prolongée
Performances améliorées dans les gommes et les boissons
3.3 Probiotiques lyophilisés vs. probiotiques lyophilisés
Lyophilisé :
Le plus stable
Idéal pour les compléments alimentaires
Survivre à température ambiante
Séché à la chaleur :
Moins cher
Nécessite une réfrigération
Moins adapté à la distribution mondiale
Les marques de haute qualité choisissent toujours des variétés lyophilisées.
3.4 Formes gélifiées et liquides
Les consommateurs adorent les gommes à mâcher, mais l'incorporation de probiotiques dans les gommes à mâcher est techniquement difficile car :
Les gommes contiennent de l'humidité
La chaleur dégagée lors de la production peut tuer les bactéries
La viabilité à long terme est plus difficile à maintenir
Cela dit, la technologie de microencapsulation a considérablement amélioré la stabilité des gommes.
Cependant, les gommes à mâcher offrent généralement un nombre d'UFC plus faible et moins de choix de souches.
4. Sécurité, effets secondaires et contre-indications
Les probiotiques sont généralement considérés comme sûrs pour les personnes en bonne santé.
Cependant, certains groupes nécessitent une attention particulière.
4.1 Effets secondaires courants et bénins (généralement temporaires)
Gaz
Ballonnements
Augmentation de la fréquence des selles
légère gêne abdominale
Ces effets disparaissent généralement après 3 à 7 jours, le temps que le microbiome s'adapte.
4.2 Qui doit être prudent ?
Les probiotiques peuvent présenter des risques pour :
Patients immunodéprimés
Les personnes sous chimiothérapie
Personnes porteuses de cathéters veineux centraux
Les personnes atteintes de pancréatite sévère
Patients hospitalisés en soins intensifs
Ces groupes de personnes ne devraient prendre des probiotiques que sous surveillance médicale.
5. Comment choisir un supplément probiotique de haute qualité
La plupart des consommateurs choisissent leurs probiotiques en fonction des arguments marketing, ce qui engendre souvent déception. Une marque de compléments alimentaires sérieuse ou un utilisateur averti devrait évaluer les probiotiques selon les critères suivants :

5.1 L'étiquette doit indiquer le nom complet de la souche
Pas seulement Lactobacillus , pas seulement L. rhamnosus , mais l'identification complète de la souche, par exemple :
L. rhamnosus GG
B. infantis 35624
S. boulardii CNCM I-745
Si la souche est absente, le produit n'est pas un probiotique scientifiquement validé.
5,2 UFC garanties à la date de péremption (et non à la fabrication)
Les probiotiques de haute qualité précisent :
« X milliards d’UFC à la date de péremption. »
Les marques de mauvaise qualité ne garantissent le nombre d'UFC qu'à la date de fabrication.
5.3 Technologie de livraison
Choisissez des probiotiques contenant :
Enrobage entérique
Microencapsulation
emballage déshydratant
Évitez les produits dont les allégations de stabilité ne sont pas claires.
5.4 Tests effectués par des tiers
Les compléments alimentaires haut de gamme fournissent :
Pureté microbienne
Tests de métaux lourds
dépistage des agents pathogènes
données sur la durée de conservation
Les marchés internationaux exigent souvent un COA (Certificat d'Analyse).
5.5 Évitez les « formules fourre-tout »
Certaines marques ajoutent 20 à 30 souches sans aucune preuve.
Plus de souches ≠ meilleurs résultats.
Une formule bien étudiée de 3 à 6 souches surpasse souvent un mélange aléatoire de 20 souches.
Prébiotiques, symbiotiques, interactions alimentaires et perspectives futures de la science du microbiome
1. Probiotiques vs Prébiotiques vs Synbiotiques : Analyse scientifique complète
Comprendre les différences entre probiotiques, prébiotiques et symbiotiques est essentiel pour concevoir des compléments alimentaires efficaces et répondre aux attentes des consommateurs. Bien que ces trois éléments soient souvent commercialisés ensemble, ils jouent des rôles biologiques totalement différents au sein de l'écosystème intestinal.
1.1 Que sont les prébiotiques ?
Les prébiotiques sont des fibres et des composés non digestibles qui nourrissent sélectivement les bactéries bénéfiques de l'intestin. Contrairement aux probiotiques, qui sont des organismes vivants, les prébiotiques sont des substrats , c'est-à-dire qu'ils servent de « source de nourriture » aux micro-organismes souhaitables.
Exemples :
Fructooligosaccharides (FOS)
Galactooligosaccharides (GOS)
Inuline
Xylooligosaccharides (XOS)
Amidon résistant
Certains polyphénols (par exemple, ceux provenant des baies, du thé vert, du cacao)
Les prébiotiques stimulent la production d'acides gras à chaîne courte (AGCC), notamment le butyrate , qui est fortement lié à la régulation métabolique, à la fonction de barrière intestinale, à l'équilibre immunitaire et même aux performances cognitives.
Point clé :
Les prébiotiques agissent lentement mais efficacement. Ils constituent le fondement d'un microbiome sain à long terme.
Sans un apport suffisant en fibres, les suppléments probiotiques ne peuvent pas fonctionner de manière optimale, car les bactéries bénéfiques manquent du carburant dont elles ont besoin pour coloniser ou influencer l'environnement intestinal.
1.2 Que sont les synbiotiques ?
Les synbiotiques associent probiotiques et prébiotiques dans une formulation unique qui améliore la survie et l'expression des souches probiotiques.
Il en existe deux types :
Synbiotiques complémentaires
Les prébiotiques favorisent la croissance d'une plus grande variété de bactéries bénéfiques, et pas nécessairement de la souche probiotique exacte présente dans le produit.
Exemple : L. plantarum + inuline.
Synbiotiques synergiques
Le prébiotique est spécifiquement sélectionné pour favoriser la croissance ou l'activité métabolique de la souche probiotique incluse.
Exemple : B. infantis + GOS (son substrat préféré).
Les symbiotiques peuvent :
Améliorer le succès de la colonisation
Augmenter la production d'AGCC
Améliorer la régularité des selles
Améliorer la fonction immunitaire
Favoriser l'équilibre métabolique
Favoriser des changements plus stables du microbiome
Ils sont particulièrement précieux pour les personnes ayant une faible consommation de fibres alimentaires, une utilisation fréquente d'antibiotiques ou des problèmes digestifs chroniques.
2. Comment l'alimentation influence l'efficacité des probiotiques
Les probiotiques n'agissent pas isolément. Leur efficacité dépend fortement de l'environnement alimentaire de l'hôte. L'alimentation détermine le « terrain » dans lequel les probiotiques tentent de se développer.
Voici les interactions les plus fortes entre l'alimentation et le microbiome étayées par la recherche :
2.1 L'apport en fibres est le principal facteur déterminant de la diversité du microbiome.
Les populations ayant une alimentation riche en fibres (communautés africaines traditionnelles, adeptes du régime méditerranéen) présentent :
Diversité microbienne plus élevée
Production accrue d'AGCC
Diminution des taux de maladies métaboliques
Intégrité renforcée de la barrière intestinale
Lorsque l'apport en fibres alimentaires est insuffisant, les bactéries bénéfiques meurent de faim, ce qui entraîne une dysbiose, même chez les personnes prenant des probiotiques.
Autrement dit:
Un complément probiotique ne peut pas compenser un régime alimentaire pauvre en fibres.
Mais dans un environnement riche en fibres, les probiotiques se développent et produisent des résultats nettement supérieurs.
2.2 Les aliments riches en sucre et transformés endommagent le microbiome
Régimes riches en sucres raffinés et en graisses transformées :
Réduire les bactéries bénéfiques
Augmenter les microbes tolérants à la bile et liés à l'inflammation
Perturber la signalisation de l'axe intestin-cerveau
Favoriser l'hyperperméabilité intestinale
Risque accru de pathologies liées à la dysbiose
Même les meilleures souches probiotiques ne peuvent pas contrer durablement l'inflammation alimentaire si l'alimentation de base reste hautement transformée.
2.3 Aliments fermentés vs suppléments probiotiques
Les aliments fermentés (yaourt, kéfir, kimchi, kombucha, choucroute, miso, tempeh) contiennent des microbes vivants, mais :
Les souches correspondent rarement aux souches probiotiques cliniques.
Le nombre d'UFC varie considérablement.
De nombreux micro-organismes ne survivent pas à l'acidité gastrique.
Les effets sont plus légers et moins ciblés.
Les aliments fermentés favorisent la diversité globale du microbiome et la richesse alimentaire, mais ne remplacent pas les suppléments probiotiques validés cliniquement.
3. Combien de temps faut-il pour que les probiotiques agissent ? Un calendrier réaliste
De nombreux consommateurs s'attendent à ce que les probiotiques agissent en quelques jours, mais le délai réel dépend de plusieurs facteurs :
3.1 Effets à court terme (0 à 2 semaines)
Les utilisateurs peuvent rencontrer les problèmes suivants :
Légers changements digestifs (gaz, modifications du transit intestinal)
Amélioration de la régularité des selles
Réduction des ballonnements
Meilleure tolérance à certains aliments
Ces changements reflètent les premières interactions et adaptations microbiennes.
3.2 Effets à moyen terme (3 à 6 semaines)
Les bienfaits des probiotiques deviennent plus perceptibles :
Réduction des symptômes du syndrome du côlon irritable
Diminution de la fréquence des crises digestives
résilience immunitaire accrue
Amélioration de la stabilité du microbiome vaginal
Meilleure stabilité de l'humeur et réponse au stress
Cette phase reflète une colonisation stabilisée et une modulation immunitaire.
3.3 Effets à long terme (2 à 6 mois)
Des changements profonds, induits par le microbiome :
Diversité microbienne plus élevée
barrière intestinale plus résistante
Amélioration des marqueurs métaboliques
Réduction de l'inflammation systémique
Un bien-être mental et émotionnel plus stable
Améliorations durables de la digestion
Ces effets nécessitent de la constance et des habitudes alimentaires adaptées.
4. Orientations futures en sciences des probiotiques et du microbiome
Le domaine des probiotiques évolue rapidement. La prochaine décennie apportera des avancées révolutionnaires qui dépasseront largement la génération actuelle de compléments alimentaires.
4.1 Probiotiques de précision (personnalisation au niveau de la souche)
Le séquençage génomique permet aux chercheurs d'identifier des souches très spécifiques adaptées aux profils microbiens individuels. Les futurs probiotiques seront personnalisés , et non universels.
4.2 Postbiotiques : la prochaine génération de thérapies microbiennes
Les postbiotiques sont des produits microbiens non vivants , notamment des métabolites, des enzymes, des peptides et des fragments cellulaires.
Ils offrent des avantages :
Aucun problème de survie
Très stable
Mécanismes clairs
Effets immunomodulateurs puissants
Les postbiotiques pourraient bientôt surpasser les probiotiques traditionnels dans certaines applications thérapeutiques.
4.3 Produits biothérapeutiques vivants (PBV)
Les LBP sont des microbes de qualité pharmaceutique conçus comme des médicaments réglementés , et non comme des compléments alimentaires.
Elles ciblent des affections telles que :
Rectocolite hémorragique
maladie de Crohn
Infections résistantes aux antibiotiques
Troubles métaboliques
Ce domaine va redéfinir notre utilisation des micro-organismes à des fins thérapeutiques.
4.4 Thérapies cognitives et de l'humeur basées sur le microbiome
« Psychobiotiques » s’étendra à :
Soutien en cas d'anxiété et de dépression
Optimisation du sommeil
Amélioration des performances cognitives
Gestion des affections neuro-inflammatoires
Les premières recherches sont très prometteuses.
4.5 Recherche sur le microbiome et la longévité
Des études récentes suggèrent que le microbiome influence :
Taux de vieillissement
Maintien musculaire
Équilibre hormonal
Inflammation (« inflammaging »)
Maladies liées à l'âge
Les probiotiques pourraient devenir à l'avenir des éléments essentiels des stratégies anti-âge.
5. Résumé final : Ce que les probiotiques offrent réellement
Les probiotiques ne sont pas des pilules magiques, mais bien choisis, associés à une alimentation équilibrée et pris régulièrement, ils procurent des bienfaits considérables, étayés par des décennies de recherche scientifique.
Une stratégie probiotique de très haute qualité implique :
Spécificité de la souche
CFU adéquats
Technologie de livraison robuste
Soutien prébiotique
Sélection personnalisée
Cohérence à long terme
Attentes fondées sur des preuves
Le microbiome est au cœur de la santé humaine : il influence le système digestif, immunitaire, métabolique, mental et même cutané. Le soutenir par des probiotiques ciblés est l’une des méthodes les plus efficaces et scientifiquement prouvées pour améliorer la santé à long terme.
Liste de référence
1. Directives FAO/OMS sur les probiotiques
FAO/OMS. (2002). Lignes directrices pour l’évaluation des probiotiques dans les aliments .
https://www.fao.org/3/a0512e/a0512e.pdf
2. NIH – Centre national pour la santé complémentaire et intégrative (NCCIH)
Probiotiques : ce que vous devez savoir
https://www.nccih.nih.gov/health/probiotics-what-you-need-to-know
3. ISAPP – Association scientifique internationale pour les probiotiques et les prébiotiques
Déclarations de consensus et ressources scientifiques
https://isappscience.org
4. Lactobacillus rhamnosus GG (ATCC 53103)
Szajewska H. et al., The Lancet Infectious Diseases , 2015.
Index PubMed : https://pubmed.ncbi.nlm.nih.gov/25547277/
5. Lactobacillus plantarum 299v – Recherche sur le syndrome du côlon irritable
Johansson ML et al. Étude clinique sur le SII.
Recherche PubMed : https://pubmed.ncbi.nlm.nih.gov/?term=Lactobacillus+plantarum+299v
6. Bifidobactérie infantile 35624
Whorwell PJ et al., Gastroentérologie , 2006.
https://pubmed.ncbi.nlm.nih.gov/16401471/
7. Saccharomyces boulardii CNCM I-745
McFarland LV, Progrès thérapeutiques en gastro-entérologie .
https://pubmed.ncbi.nlm.nih.gov/?term=Saccharomyces+boulardii+CNCM+I-745
8. Psychobiotiques : L. helveticus R0052 & B. longum R0175
Messaoudi M. et al., British Journal of Nutrition , 2011.
https://pubmed.ncbi.nlm.nih.gov/21736802/
9. Recherche sur l'axe intestin-cerveau – Cryan et Dinan
Études fondamentales :
https://pubmed.ncbi.nlm.nih.gov/?term=Cryan+Dinan+microbiome
10. Recherche sur les probiotiques infantiles (B. infantis)
Centre de recherche sur le lait maternel et l'allaitement de l'UC Davis
https://hmnb.ucdavis.edu
11. Lactobacillus reuteri DSM 17938 pour les coliques du nourrisson
https://pubmed.ncbi.nlm.nih.gov/?term=Lactobacillus+reuteri+DSM+17938
12. Santé des femmes – Souches GR-1 et RC-14
Reid G. et al., Journal des maladies infectieuses .
https://pubmed.ncbi.nlm.nih.gov/?term=Reid+GR-1+RC-14
13. Santé métabolique – Lactobacillus gasseri SBT2055
https://pubmed.ncbi.nlm.nih.gov/?term=Lactobacillus+gasseri+SBT2055
14. Bifidobacterium breve B-3
https://pubmed.ncbi.nlm.nih.gov/?term=Bifidobacterium+breve+B-3
15. Recherche sur la barrière intestinale et les acides gras à chaîne courte (AGCC)
https://pubmed.ncbi.nlm.nih.gov/?term=SCFA+gut+barrier
16. EFSA (Autorité européenne de sécurité des aliments)
Liste de présomption de sécurité qualifiée
https://www.efsa.europa.eu
17. Avis de la FDA concernant le statut GRAS des ingrédients probiotiques
https://www.fda.gov/food/generally-recognized-safe-gras
18. ClinicalTrials.gov – Essais cliniques sur les probiotiques
https://clinicaltrials.gov
19. Recherche dans la base de données PubMed – Base de données générale sur les probiotiques
https://pubmed.ncbi.nlm.nih.gov/?term=probiotics






